Käfige aus dem Kolben
Archivmeldung vom 22.09.2006
Bitte beachten Sie, dass die Meldung den Stand der Dinge zum Zeitpunkt ihrer Veröffentlichung am 22.09.2006 wiedergibt. Eventuelle in der Zwischenzeit veränderte Sachverhalte bleiben daher unberücksichtigt.
Freigeschaltet durch Thorsten SchmittElektronische Bauteile verdanken ihre Rechenkraft und ihre Speicherkapazität Halbleitern wie Silizium. Künftig könnte auch eine spezielle Form des Germaniums, in der seine Struktur aus einem Netz geräumiger Käfige aufgebaut ist, als Ausgangsmaterial für elektronische Bauelemente dienen - das zumindest sagen theoretische Untersuchungen voraus.
Jetzt haben Wissenschaftler des Max-Planck-Instituts für Chemische Physik fester Stoffe einen Weg gefunden, diese neue, metastabile Modifikation des Elements Germanium auf relativ einfache Weise und in größeren Mengen herzustellen. (Nature, 21. September 2006)
Abb.1: Käfigstruktur von
Clathrat-II Germanium: In der elektronenmikroskopischen Abbildung erscheinen
Atome dunkel, die Zwischenräume hell. Eine Computersimulation bestätigt das
experimentelle Ergebnis (oben links eingefügt).
Ihre besondere Struktur gibt Clathraten besondere Eigenschaften:
In den Käfigen, aus denen sie sich aufbauen, können sie etwa Atome anderer
Elemente beherbergen, die die thermische Leitfähigkeit der Verbindungen
beeinflussen. Daher eignen sie sich möglicherweise, um Thermoelektrika
herzustellen, die Temperaturunterschiede in Strom verwandeln oder als
Peltierelemente wie kleine Kühlaggregate wirken. Leere Clathrate eigenen sich
dagegen anders als die bekannten Formen von Silizium und Germanium als
Ausgangsstoff für optoelektronische Bauelemente wie Photodioden. Zumindest
theoretisch.
Praktisch ließen sich die vielversprechenden Formen der Halbleiter bislang - wenn überhaupt - nur mit großem Aufwand herstellen. Jetzt haben die Max-Planck-Wissenschaftler aber einen überraschend einfachen Weg gefunden, Germanium in die käfigförmige Struktur zu bringen: Sie haben reaktive Verbindungen des Elements mit Natrium oder Kalium zu einer neuen Form des Elements reagieren lassen. Nach ihrem Rezept können die Dresdener Chemiker sowohl Clathrate mit leeren Käfigen synthetisieren als auch solche, in deren Hohlräumen Atome anderer Elemente sitzen.
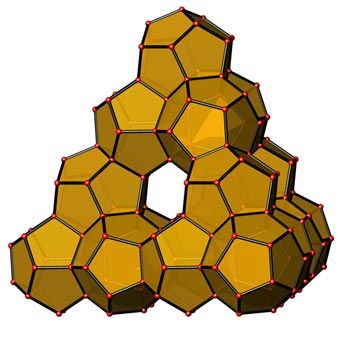
Abb. 2: Clathrat-II Germanium ist eine
neue Modifikation des Elements Germanium und setzt sich aus Polyedern mit 20
bzw. 28 Germaniumatomen (rot) zusammen. Die kleineren Polyeder (gelb) bilden so
genannte Supertetraeder mit großen Hohlräumen.
Den Wissenschaftlern kam dabei der Zufall zu Hilfe, der ihnen
eine effektivere und preiswerte Methode bescherte, um Clathrate zu
synthetisieren. "Wir suchten eigentlich nach Lösungsmitteln für Zintl-Phasen
dieser Elemente", sagt Michael Baitinger, der in der Abteilung von Prof.Yuri
Grin an den Untersuchungen an Clathraten beteiligt war. Diese Silizium-
beziehungsweise Germanium-Verbindungen, in denen die Halbmetalle ein ziemlich
gespanntes negativ geladenes Atomgerüst bilden, reagieren auf Luft und Wasser
sehr empfindlich - manche zersetzen sich sogar explosionsartig. Daher lösten die
Wissenschaftler die Verbindungen in flüssigen organischen Salzen wie
Dodecyltrimethylammoniumchlorid (DTAC).
"Dabei stellten wir fest, dass
das DTAC die Zintl-Phasen bei relativ milden 300 Grad in Clathrate verwandeln.
In nur zwei Tagen und mit Methoden, die in der organischen Chemie weit
verbreitet sind." Diese Methoden machen die Synthese nicht nur preiswert,
sondern eignen sich auch, um Clathrate in großem Maßstab zu produzieren oder in
dünnen Schichten auf einem Trägermaterial abzuscheiden. Viel wichtiger ist für
die Chemiker aber zunächst, dass sie einen prinzipiellen Weg gefunden haben, um
aus leicht herstellbaren reaktiven Ausgangsverbindungen käfigförmige Strukturen
aus Silizium oder Germanium zu erzeugen..
Normalerweise erhalten
Chemiker Silizium- oder Germaniumclathrate nur bei sehr viel höheren
Temperaturen, und auch die Reaktionszeiten sind deutlich länger. Da viele
Clathrate jedoch metastabil sind, können sie bei höheren Temperaturen erst gar
nicht entstehen. So wandelt sich auch Clathrat-II Germanium bei Temperaturen
über 500 Grad in die bekannte Form α-Germanium um. Daher ist es über
herkömmliche Hochtemperatursynthesen nicht zugänglich.
Um die
überraschende Existenz von Clathrat-II Germanium zu belegen, haben die
Wissenschaftler das Produkt anschließend mit einer ganzen Palette von
Instrumenten untersucht: Elektronenbeugung (SAED) und hochauflösender
Transmissionselektronenmikroskopie (HRTEM), um die Struktur aufzuklären,
energiedispersiver Röntgenspektroskopie (EDXS) und Elektronen-Energieverlust
Spektroskopie (EELS), um die Zusammensetzung herauszufinden.
Originalveröffentlichung:
Arnold M. Guloy, Reiner Ramlau, Zhongjia Tang, Walter Schnelle, Michael
Baitinger and Yuri Grin
A guest-free germanium
clathrate
Nature, 21. September 2006
Quelle: Pressemitteilung Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V.